Поздрави жителите на нашия сайт!
От година на година производството на петрол става все по-сложно, а горивото, получено от него, става все по-скъпо. В страните от ЕС като цяло заплашват да спрат производството на бензинови двигатели, искат да заменят всички превозни средства с електрически автомобили. Но литиевите батерии все още са далеч от идеалния и между другото, изобщо не бързат да станат идеални. В най-добрия случай при едно зареждане на литиева батерия ще бъде възможно да се измине разстояние от максимум 700 км, след което ще трябва да зареждате батерията за около седмица, а ако използвате обикновен контакт за зареждане, това обикновено отнема много време. И само си представяте какво ще се случи, ако всеки започне постоянно да зарежда електрическите си автомобили, какви огромни товари ще бъдат в електрическата мрежа и колко напрежение ще се източи. Като цяло бъдещето на литиевите батерии все още е доста неясно и всяка година все повече и повече изследвания се отделят на търсенето на нови опции за батерията.
Както знаете, най-енергоемкият метал е алуминият. Вече в наше време по някои прототипи на алуминиеви батерии можете да изминете около 2000 км без презареждане, а презареждането на този тип батерии отнема само 15 минути, след което можете да продължите още около 2000 км.
Презареждането на алуминиеви батерии се различава от презареждането на литиеви батерии. Независимо от това, в него няма нищо сложно, просто трябва да поставите нов алуминий, да излеете електролита и да сипете нов електролит, всичко по същество е същото като бензин кола, само това е електрически автомобил и няма никакви натоварвания в електрическата мрежа. Освен това не е необходимо да произвеждате огромен брой контакти с проводници с огромно напречно сечение, за да заредите всички тези електрически автомобили.
Но не всичко тук е толкова гладко. Получаването на електричество от алуминий изобщо не е толкова лесно, колкото бихме искали. Първо, нека разберем какъв е принципът на алуминиево-въздушната батерия.
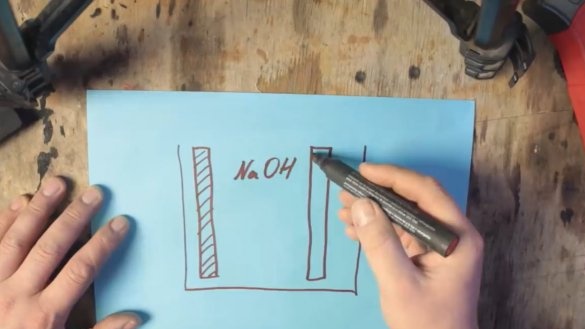
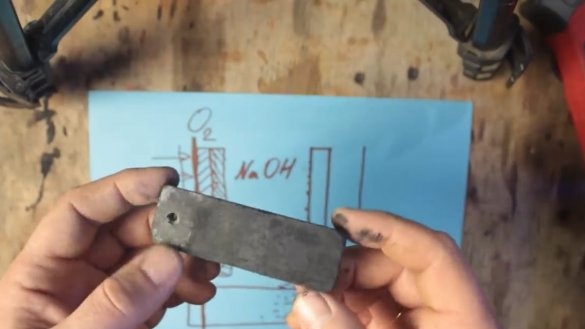
За да започне да работи такава батерия, ще са необходими 2 електрода: един естествено от алуминий, а вторият от графит. И двата електрода са в електролитен разтвор.
Солта (NaCl) може да се използва като електролит, но с нея можете да повишите напрежението до около 0.7V. Напрежението на алкален електролит (NaOH) може да бъде повишено вече повече, до около 1V.
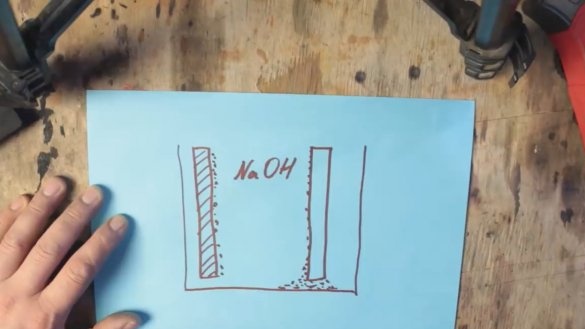
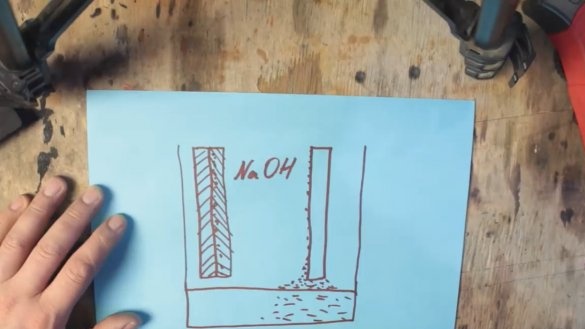
По време на химическата реакция алуминият се покрива със слой алуминиев хидроксид (Al (OH) 3), който постепенно потъва до дъното на резервоара. И на повърхността на графитния електрод се образуват водородни мехурчета, което от своя страна води до увеличаване на съпротивлението и спад на напрежението, този процес се нарича поляризация.
Първият проблем с утаяването на алуминиевия хидроксид може да бъде отстранен чрез просто увеличаване на капацитета, където отработеният продукт ще се утаи, но вторият проблем може да бъде подпомогнат от деполяризираща маса на базата на манганов оксид, която по време на работа ще се превърне в манганов хидроксид.
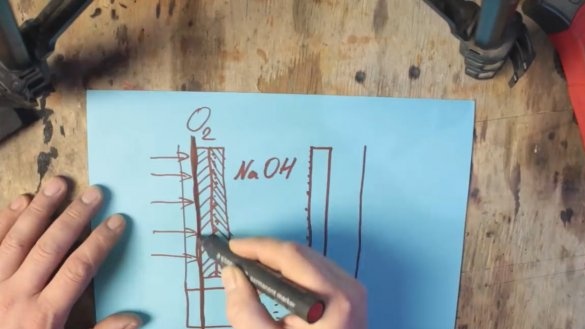
Всъщност имахме обикновена алкална батерия, но само много голяма. Но възниква нов проблем. Факт е, че се консумира и манганов оксид и той също трябва да бъде сменен. И трябва да гарантираме, че се изразходва само алуминий. За целта вземете кислород от околния въздух. От тук започва батерията с алуминиев въздух. Една от стените просто трябва да бъде заменена с газопроницаема мембрана, а графитният електрод трябва да бъде заменен със смес от графит и манганов оксид с платинени или сребърни наночастици.
Манганов оксид с наночастици от благороден метал не реагира, а действа като катализатор, поради което водородът от електролита се окислява от кислорода във въздуха.
Технологията за производство на манганов оксид с включвания на сребърни наночастици по принцип не е сложна и може да бъде изпробвана в занаятчийски условия. Но в тази статия ще обсъдим как да направите най-бюджетния вариант за батерия, която получава енергия от алуминий. Следните инструкции са взети от Fiery TV канал YouTube. Повече подробности в оригиналното видео на автора:
Максимално бюджетната версия на графита е летни контактни вложки за тролейбуси. Можете да ги намерите абсолютно безплатно на крайните спирки на тролейбусите или можете да ги купите, не са скъпи, авторът ги намери в продажба по 22 рубли на брой.
На следващо място се нуждаем от алкал. Ето един инструмент за почистване на тръби в състава му съдържа сто процента натриева алкал.
За да започнем алкалната реакция, ни трябва само малко, 1 g алкал на 0,5 l вода ще бъде достатъчен.
На първо място, нека проверим дали наистина е необходим графитен електрод в тази батерия. За опит, нека вземем този електрод от неръждаема стомана.
Сега поставяме алуминиевата плоча и електрода от неръждаема стомана в алкала, свързваме мултицета и виждаме колко волта се оказва.
Както можете да видите, оказа се, че е около 1.4V. Сега нека проверим тока на късо съединение.
Токът на късо съединение се оказа в областта на 20mA. Какви изводи могат да се направят: теоретично при екстремни условия е възможно да се сглоби батерия от халби от неръждаема стомана и алуминиево фолио.
След това ще имаме меден електрод, изработен от електрическа мед.
Както можем да наблюдаваме, напрежението се оказа малко по-високо от 1,4 V, но токът на късо съединение в началото беше висок, но след това започна да провисва доста бързо и медта също започна да се покрива с тъмно покритие, най-вероятно примесите във водата предизвикват този ефект, тъй като водата В този експеримент авторът взел от крана.
Сега потопете графитния електрод в електролитния разтвор.
С този електрод се получи напрежение от 1.3 V, токът на късо съединение спря в областта на 17 mA. На пръв поглед изглежда, че електродът от неръждаема стомана е по-ефективен, но повърхността на неръждаемия електрод е по-голяма, така че все още не е известно кой графит или неръждаема стомана са по-добри.
Тъй като графитът има доста голяма устойчивост, трябва по някакъв начин да се справите с него. Необходимо е да се направят електроди от материал, който е добре проводящ, а графитът трябва да бъде само на повърхността му.Взето е решение да се пробие през графита и в получените отвори се реже резбата за болтовете m6.
Резултатът е стоманен електрод с графитна обвивка.
Съпротивлението на непробит графит е около 4,5 ома, но на пробити графит е около 1,7 ома.
На лицето, намаляване на устойчивостта и, следователно, ефективността на структурата ще се увеличи. При по-нататъшни експерименти ще използваме дестилирана вода.
Първият експеримент с електролит, в който 4 g алкали на 1 литър вода.
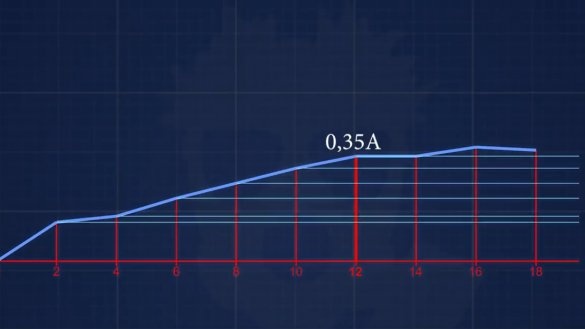
Токът на късо съединение се оказа 150mA. Следващият електролит има концентрация 6 g алкали на 1 литър. Е и така нататък, всеки път ще увеличаваме концентрацията с 2 g, докато достигнем концентрация, при която токът няма да се увеличи.
Въпреки че такава обикновена батерия няма голяма ефективност на тока, но такава батерия може да работи много дълго време и всеки алуминий може да се използва като електроди, които лесно могат да се разтопят в електроди с всякаква форма, например алуминиеви кутии различни алкохолни и безалкохолни напитки, шоколадово фолио и др.
В резултат на това след всички експерименти с различни концентрации на електролит става ясно, че при този дизайн на батерията няма смисъл да се добавят повече от 12 g алкали към 1 литър вода, тоест получаваме около 1% разтвор.
Тогава авторът сглоби още един клип, състоящ се от 3 електроди.
Две батерии дават по-високо напрежение и по-малко загуби, така че резултатът е по-добър.
Сега нека вземем кофа с електролит, голямо парче алуминий и 2 електрода от неръждаема стомана.
В кофа концентрация на електролит 10g / 1l. Максимален ток 1.3A, той спадна до 520mA. С цялата огромна площ от неръждаема стомана, тя не се сравнява с графит, защото се оказа 600mA с графит. Между другото, по време на реакцията се отделя водород, който също може да бъде събран и използван като източник на енергия. Накратко, има какво да расте. Това е всичко засега. Благодаря за вниманието. Ще се видим скоро!